2025年3月20日,南京財經(jīng)大學(xué)食品科學(xué)與工程學(xué)院2021級碩士研究生馬賽(第一作者),馬高興教授(通訊作者)在國際TOP期刊Journal of Agricultural and Food Chemistry (Q1,IF: 5.7)發(fā)表題為“Effects and Mechanisms of Pleurotus eryngii Polysaccharide on Intestinal Barrier Damage: Based on the Perspective of Its Interaction with Intestinal Mucus during Gut Digestion”的研究性論文。
杏鮑菇多糖(Pleurotus eryngii polysaccharides, PEPs)是一種具有豐富功能活性的食源性菌物多糖,研究初期,團(tuán)隊深入分析了具PEPs的免疫調(diào)節(jié)活性,并研究了PEPs在體內(nèi)和體外的消化和發(fā)酵特性,進(jìn)而利用葡聚糖硫酸鈉(DSS)誘導(dǎo)的小鼠腸炎模型觀察了PEPs與腸道微生物群之間的相互作用對結(jié)腸炎的改善作用,但并未對相關(guān)機制進(jìn)行深入解析。
當(dāng)前,關(guān)于腸道第一道屏障,腸粘液(IMs)層對PEPs活性的影響研究較少。具體而言,由于PEPs結(jié)構(gòu)和代謝過程的復(fù)雜性,以及PEPs必須通過各種腸道屏障才能接觸細(xì)胞或進(jìn)入循環(huán)系統(tǒng),因此有必要研究它們在腸道粘液層中的行為和變化。團(tuán)隊前期研究分析了PEPs和IMs在體外相互作用的理化性質(zhì),并鑒于物質(zhì)結(jié)構(gòu)與功能之間的關(guān)系,初步發(fā)現(xiàn)了與IMs的相互作用可能會影響PEPs的功能活性。
基于前期基礎(chǔ),研究采用了體外模擬消化和發(fā)酵模型來獲得PEPs相關(guān)腸道消化和腸道菌群酵解產(chǎn)物,進(jìn)一步研究了相關(guān)產(chǎn)物與IMs的相互作用對腸道屏障損傷的潛在保護(hù)作用;此外,利用體內(nèi)動物模型,研究了在DSS 誘導(dǎo)的腸屏障損傷模型中,不同的PEPs攝入時間對其與粘蛋白之間相互作用特征的影響;最后探討了在IMs介導(dǎo)的情況下,PEPs對腸道屏障損傷的保護(hù)作用機制。

研究亮點
1. 采用細(xì)胞模型研究PEPs與IMs復(fù)合物對腸道屏障損傷的保護(hù)作用。
2. 探究PEPs與IMs在體內(nèi)的相互作用特征,并解析PEPs在IMs的介導(dǎo)下對腸屏障損傷的影響。
3. 評估相互作用特征與腸屏障損傷程度之間的關(guān)系,并從消化和發(fā)酵的角度研究基于IMs作用下PEPs在腸道中的活性作用機理。
研究結(jié)論
IMs和PEPs之間的相互作用會導(dǎo)致PEPs的結(jié)構(gòu)發(fā)生變化,從而改變其在腸道中的功能活性作用途徑。具體來說,Ims穩(wěn)態(tài)對PEPs改善DSS誘導(dǎo)的腸道屏障損傷影響顯著,表現(xiàn)在腸道通透性、粘蛋白和TJs蛋白分泌增加,以及NF-κB和MAPK通路中關(guān)鍵蛋白的磷酸化減少。
圖文賞析
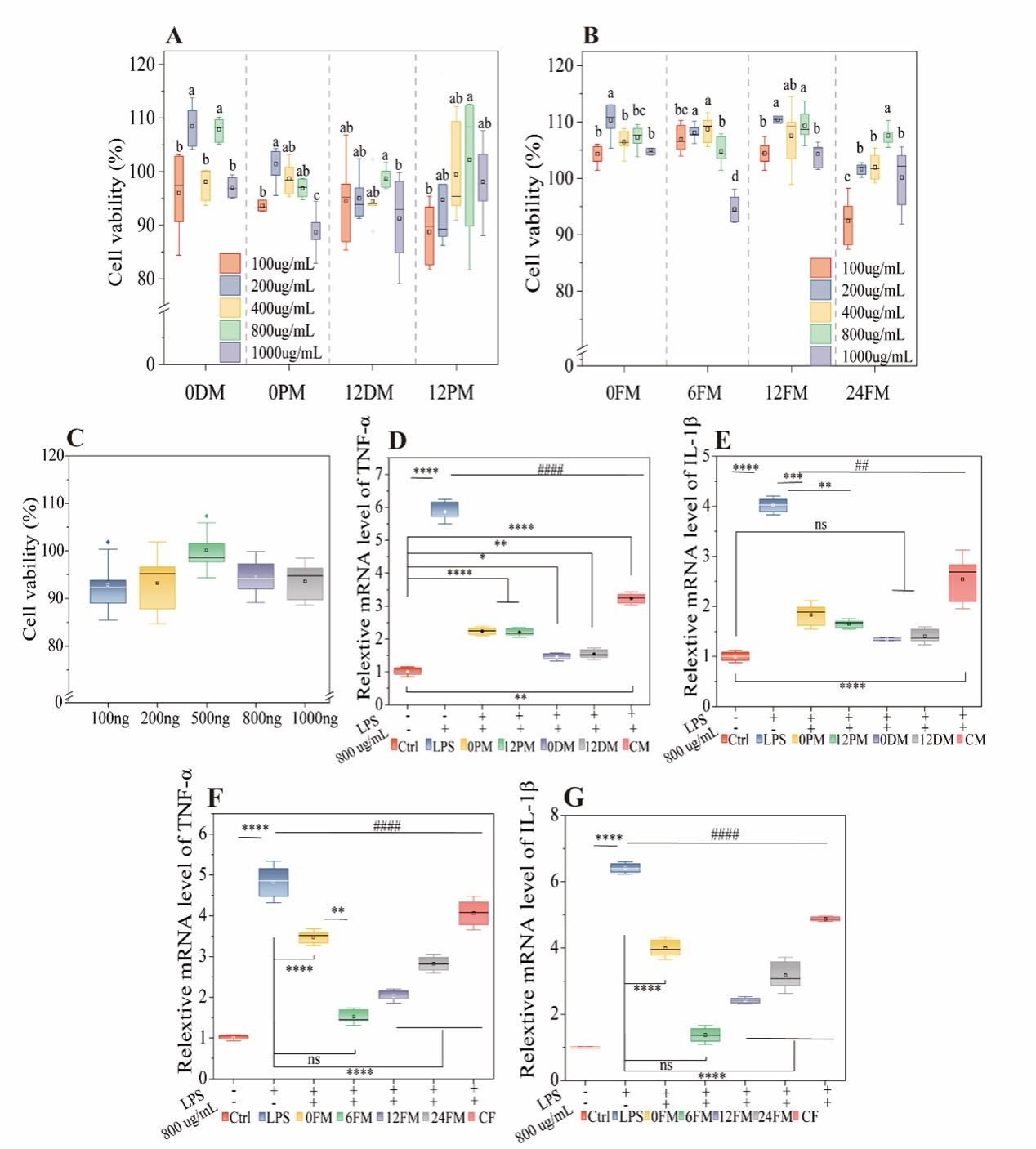
圖1各組的細(xì)胞活力比較(n=8)(A-C)。復(fù)合物對炎癥因子的影響,消化產(chǎn)物和粘蛋白復(fù)合物(D-E);發(fā)酵產(chǎn)物和粘蛋白復(fù)合物(F-G)。
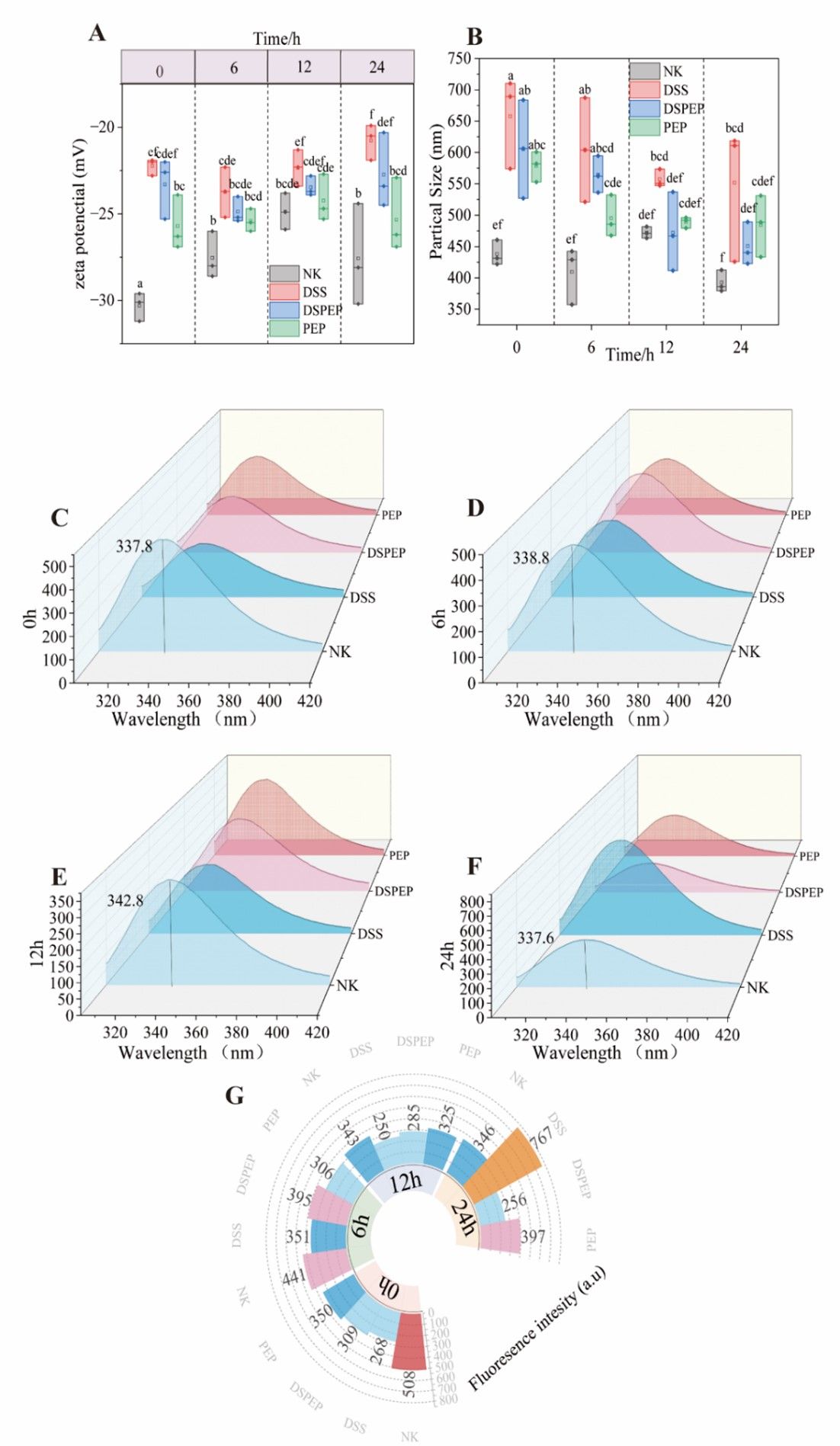
圖2 不同攝入時間的腸粘液和多糖復(fù)合物的體內(nèi)相互作用特征。Zeta 電位(A);粒徑(B);熒光光譜(C-F);熒光強度(G)。
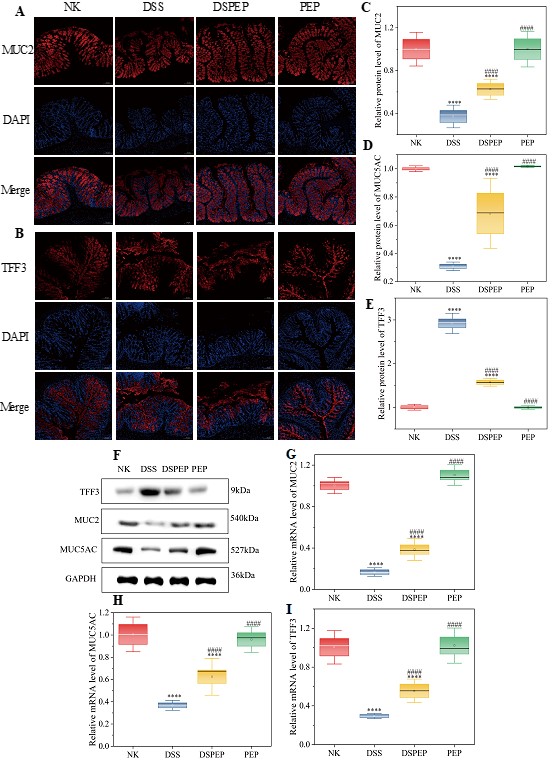
圖3 多糖對腸粘液介導(dǎo)的結(jié)腸炎中腸道粘蛋白分泌的影響,MUC2(A);TFF3(B);粘蛋白的蛋白水平(C-F);mRNA 水平(G-I)。

圖4 ZO-1(A)、occludin(B)和cadherin-1(C)的免疫熒光圖像;緊密連接蛋白的免疫印跡分析(D-G)和mRNA表達(dá)水平(H-J)。

圖5 小鼠腸道屏障損傷生物標(biāo)志物與PEPs和IMs互作特征的相關(guān)性分析。

圖6 結(jié)論可視化剖析圖
原文鏈接:https://pubs.acs.org/doi/10.1021/acs.jafc.4c11339
